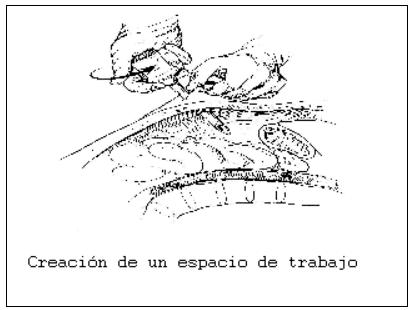
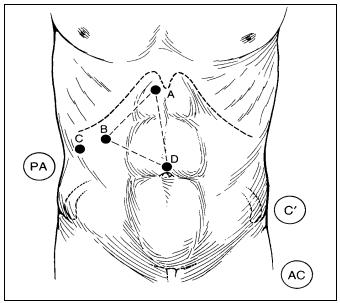
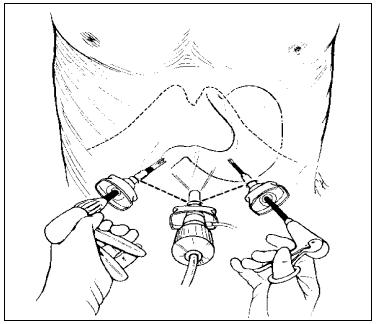
Muchos pacientes sometidos a operaciones planeadas soportan el breve período de catabolismo y ayuno sin dificultades.
La conservación de un régimen nutricional adecuado suele tener importancia crítica en pacientes quirúrgicos gravemente enfermos, con disminución ponderal y disminución de las reservas de energías preexistentes.
Es sabido que tanto las infecciones agudas como las crónicas pueden producir una depleción de las reservas corporales de nutrientes y causar deficiencia nutricional, con el posible aumento de la susceptibilidad a las infecciones secundarias o sobreañadidas.
Es sabido también que la mal nutrición grave proteíno-calórico dificulta los mecanismos de defensa inespecíficos.
Los carbohidratos, proteínas y grasas son las tres fuentes de energía de los humanos. Las reservas de carbohidratos, que consisten ante todo en el glucógeno hepático y muscular, son relativamente escasas y satisfarían las necesidades calóricas basales de menos de un día, las proteínas son una fuente mucho más abundante de energía, pero, toda pérdida de proteínas representa la pérdida de una función esencial.
Las proteínas al igual que el glucógeno, son una fuente ineficaz de energía.
Las grasas a diferencia de glucógeno y proteínas, se almacenan en un estado relativamente anhidro, de modo que son una fuente rica de energía con un aporte de 9 Kcal./g.
Ayuno:
Durante los primeros días de ayuno completo, las grasas y proteínas corporales satisfacen las necesidades calóricas; gran parte de las pequeñas reservas de glucógeno no se ven afectadas.
La administración de al menos 100 gs. de glucosa evita la mayor parte de la gluconeogénesis y reduce la pérdida de nitrógeno al menos en la mitad. El aumento leve de la insulinemia reduce la liberación de aminoácidos en los músculos, su extracción por el hígado y la gluconeogénesis.
En caso de que el ayuno completo persista varios días, el cerebro comienza a utilizar las grasas como fuente de energía. El uso de ácidos cetónicos, de origen hepático y que cruzan con facilidad la barrera hemato-encefálica, sustituye poco a poco al consumo cerebral de glucosa.
Operaciones, traumatismo y sepsis:
Los lesionados tienen aumentos variables pero obligados en el gasto de energía y la excreción de nitrógeno. Este aumento del catabolismo proteínico tarde o temprano origina insuficiencia grave de órganos.
SECUENCIA DE LOS FENOMENOS METABOLICOS Y ENDOCRINOS (Moore).
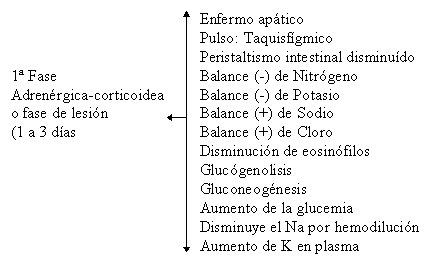
Fase catabólica:
También denominada fase adrenérgica corticoide, dado que corresponde al período en que son más importantes los cambios producidos por las hormonas adrenérgicas y los corticoides suprarrenales. En el período postoperatorio o post-traumático inmediato aumentan de manera súbita las necesidades metabólicas y la excreción urinaria de nitrógeno; los traumatismos al parecer originan la movilización obligada de proteínas para la gluconeogénesis, en la fase post-traumática inmediata y la reparación de las heridas.
El recambio de glucosa aumenta al igual que la actividad del ciclo de Cori en el que se forman compuestos intermedios de 3 carbonos, como lactato y piruvato que se convierten de nuevo en glucosa en el hígado.
También se estimula la lipólisis y es evidente la oxidación obligada de ácidos grasos en presencia de glucocorticoides, glucagon y catecolaminas, así como concentraciones bajas de insulina, o sea el estado hormonal que prevalece durante la fase catabólica de las lesiones.
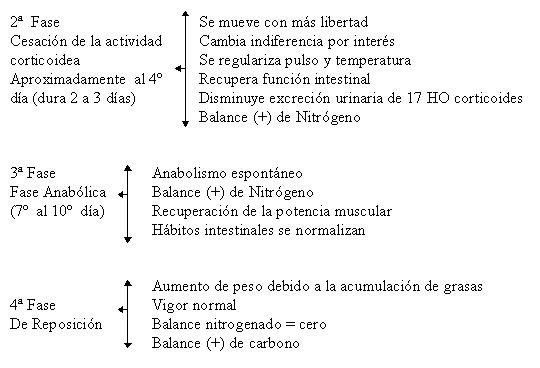
Fase Anabólica Inmediata:
El cuerpo pasa de la fase catabólica a la anabólica, según la gravedad de la lesión; puede ocurrir en 8 días en operaciones electivas sin complicaciones o al cabo de semanas en pacientes con lesiones tisulares graves, sepsis o lesiones térmicas no cubiertas con injertos. Este punto de viraje, también llamada fase de retirada corticoidea, se caracteriza por disminución notable de la excreción de nitrógeno.
Por lo general esta transición no dura más de uno o dos días y coincide con la diuresis del agua libre retenida, el interés del paciente en la ingestión de alimentos y el entorno inmediato y una mayor actividad muscular.
La fase anabólica inmediata puede durar desde unas cuantas semanas hasta varios meses, en ella aumentan en forma rápida y progresiva el peso y la fuerza muscular, el balance nitrogenado llega a un máximo.
Fase anabólica mediata:
El período final de convalecencia puede durar desde varias semanas hasta varios meses después de una lesión grave. Esta fase se acompaña de restauración gradual de las reservas adiposas conforme el balance nitrogenado positivo desciende a lo normal.
Valoración y necesidades:
Un objetivo fundamental del sostén nutricional es satisfacer las necesidades de energía para el metabolismo.
Las necesidades de energía en reposo (NER) se calculan en base a las ecuaciones Harris y Benedict:
NER(varones) = 66,47 + 13,75(P) + 5,0(T) – 6,76(A) kcal/día
NER(mujeres) = 65,51 + 9,56(P) + 1,85(T) – 4,68(A) kcal/día
| donde: | |
| P = peso (kg) | |
| T = talla (cm) | |
| A = edad (años) |
Los enfermos que reciben dietas elementales o hiperalimentación parenteral requieren complemento de vitaminas y minerales en dosis completas, vitamina K, vitamina B12 , ácido fólico.
Los complementos de oligoelementos minerales esenciales se administran por vía EV en preparados comerciales. También se suele requerir ácidos grasos esenciales, ante todo en pacientes con depleción de las reservas adiposas.
La evaluación nutricional proporciona una caracterización objetiva del estado nutricional. Existen cuatro grupos de parámetros útiles en la evaluación del estado nutritivo, son: el antropométrico, el clínico, el dietético y los datos de laboratorio.
Parámetros antropométricos
Peso corporal
Peso ideal Peso/Talla
| Porcentraje en relación al peso corporal ideal = | Peso real | x 100 |
| Peso ideal corporal |
Porcentaje en diferencia de peso
Circunferencia en el brazo
Pliegue cutáneo en el tríceps
Parámetros de laboratorio
Capacidad total de fijación de hierro (TIBC) g/dl
Transferrina sérica
Albúmina sérica Leucocitos/mm3
Linfocitos totales
Creatinina en orina de 24 hs ideal para talla de 1,70 m 1,467mg/24hs
Nitrógeno en orina en 24 hs
| Balance nitrogenado = | Ingestión de proteínas | – Nitrógeno ureico urinario |
| 6,25 |
Pruebas cutáneas
Valoran la función inmunitaria
PPD
Candidina
Dinitroclorobenceno
Necesidades calóricas y nutrientes
La dieta del paciente se hace de manera que suministre las calorías adecuadas y los nutrientes esenciales.
Los requerimientos medios para un hombre de 1,70 m de altura y 70 kg de peso variarán en condiciones normales, de 1200 a 1800 kcal/día.
Individuos sanos mantienen el equilibrio nitrogenado con una relación nitrógeno calorías totales de 1:350, los pacientes gravemente enfermos resultan beneficiados por una relación de 1:150, debido a lo comprometido de su situación proteínica.
Es necesario realizar evaluaciones a intervalos frecuentes para estar seguros del éxito del aporte nutricional.
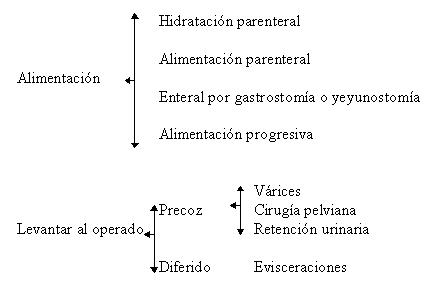
Indicaciones y métodos de sostén nutricional
La administración de volúmenes adecuados de soluciones parenterales con composición electrolítica correcta y un mínimo de 100 g/día de glucosa, para minimizar el catabolismo de proteínas, basta en muchos pacientes.
Durante la fase anabólica inmediata al paciente debe recibir ingreso calórico adecuado y de composición correcta, para satisfacer las necesidades de energía y permitir que continúe la síntesis de proteínas. Se precisa que la razón de calorías/nitrógeno sea alta, con una razón óptima de 150 kcal/g de nitrógeno.
La capacidad del organismo para tolerar y absorber los alimentos entéricos depende de su velocidad de administración, osmolalidad y composición química. La alimentación entérica con frecuencia se inicia a la velocidad de 30 a 50 ml/hora, que aumenta en 10-25 ml/h por día hasta que se administre el volumen óptimo. Después de lograr este, se aumenta poco a poco la concentración de la solución hasta que sea la necesaria.
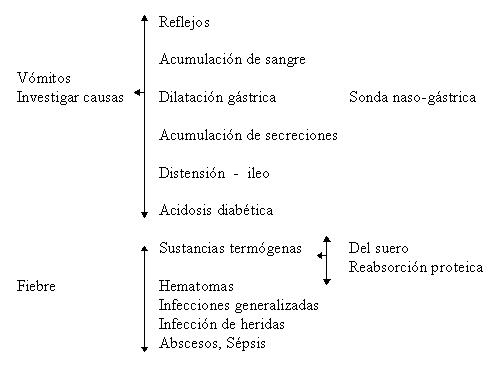
Si se prescribe la alimentación por sondas esofágicas o gástricas existe el riesgo de broncoaspiración. En caso de surgir cólicos abdominales o diarrea, es preciso disminuir la velocidad de la administración o la concentración de la solución. Todas las sondas de alimentación se han de irrigar de manera de arrastrar por completo los residuos de la solución.
Alimentación por sonda nasoentérica:
Las sondas nasoesofágicas o gástricas tiene riesgo en pacientes en quienes existe pérdida de la conciencia o de los reflejos laringeos protectores pues pueden surgir complicaciones pulmonares posiblemente mortales por broncoaspiración
La sonda faringea suele estar indicada en pacientes con tumores bucofaringeos.
La sonda naso yeyunal suele permitir la alimentación más allá de los orificios gástricos disfuncionales y fístulas gastrointestinales de localización alta, se llevan hasta la porción distal a la ubicación de la fístula en intestino mediante la colocación del paciente en posición tal que facilite el desplazamiento, se puede guiar la colocación por fluoroscopía o mediante endoscopía. Su posición correcta se confirma mediante radiografías, con medios de contraste hidrosolubles.
Alimentación por gastrostomía:
La administración de alimentos molidos por una sonda de gastrostomía es un método adecuado en pacientes con diversas lesiones gastrointestinales que surgen a la altura de la unión gastro-esofágica o arriba de esta, como por ejemplo en el carcinoma de esófago.
Por lo general se emplean las gastrostomías de Witzel, tunelizada; la de Stamm, recubierta por serosa o la de Glassman, revestida por mucosa.
La gastrostomía endoscópica percutanea ha demostrado ser un método seguro y eficaz para el sostén nutricional.
La mezcla alimentaria suele consistir en alimentos que se convierten en una mezcla semilíquida con una licuadora. La hiperosmolaridad de la fórmula alimentaria no origina problemas, a condición de que se conserve la integridad del píloro.
Alimentación por yeyunostomía:
La alimentación por yeyunostomía se suele requerir en pacientes comatosos, quienes tienen fístulas o obstrucciones gastrointestinales de localización alta o en quienes no se pueda colocar una sonda nasoyeyunal.
La yeyunostomía puede ser de tipo Roux en Y (permanente) o de Witzel (temporal). Esta última consiste en la introducción de un catéter de 18 Fr en el yeyuno proximal, la pared yeyunal se invierte sobre el catéter en unos 3 cm del punto en que sale del intestino con lo que se crea un túnel revestido por serosa que sella con rapidez el orificio yeyunal cuando se extrae el catéter. Un procedimiento opcional es la introducción por una incisión en cuadrante superior de una catéter de silastic o polietileno. El yeyuno se sutura a la pared abdominal anterior en el punto en que entra el catéter, para aislarlo de la cavidad peritoneal.
Existen sets de yeyunostomía por catéter con aguja.
En caso de que se mueva accidentalmente el catéter de yeyunostomía, están contraindicados los intentos ciegos de reinserción, se podría reintroducir bajo control fluoroscópico, pero existe riesgo de peritonitis.
En caso de dudas es preferible reintroducirlo mediante cirugía.
La alimentación comienza después de 12 a 18 hs de creada la yeyunostomía, aunque no sea audible el peristaltismo.
En caso de surgir diarrea se controla mediante disminución transitoria de la concentración y el volumen del alimento administrado, en ocasiones se interrumpe la alimentación por un día para después reanudarla desde el punto inicial del régimen alimentario, que debe progresar algo más lentamente. Si persisten diarrea o cólicos, una tableta pulverizada de clorhidrato de difenoxilato, o loperamida, o algún atropínico se administran por el catéter 30 minutos antes de la fórmula.
Si un paciente con yeyunostomía tiene fístula intestinal proximal o biliar que drenan más de 300 ml/día, el drenaje de la fístula se extrae por aspiración con bomba e instila en pequeños volúmenes durante el día. No es recomendable instilar el jugo gástrico aspirado ya que este puede causar inflamación yeyunal y diarrea abundante.
El déficit de los que se pierde por las fístulas en volúmenes que excedan la capacidad de reposición por yeyunostomía, se aporta con agua y electrolitos por vía endovenosa.
Dietas elementales:
Las dietas líquidas nutricionalmente completas que se expenden en el comercio, derivadas en forma purificada de alimentos naturales o sintéticos, han recibido nombres como los de dietas químicamente definidas o elementales.
ALIMENTACION PARENTERAL
Dudrick y cols han demostrado que es factible en clínica la satisfacción de las necesidades nutricionales completas durante largos períodos con fórmulas parenterales ricas en calorías. La alimentación parenteral consiste en la administración constante de una solución hiperosmolar, que contiene carbohidratos proteínas, grasas y otros nutrientes necesarios, por un catéter a permanencia que se coloca en la vena cava superior.
La razón de calorías/ nitrógeno debe ser adecuado (de al menos 100 a 150 kcal/g de nitrógeno), con administración simultánea de ambos. Cuando las fuentes de caloría y nitrógeno se administran por separado, disminuye en forma significativa el aprovechamiento del nitrógeno.
Indicaciones para la hiperalimentación intravenosa
Pacientes gravemente enfermos por:
Desnutrición
Sepsis
Traumatismos quirúrgicos
Traumatismos accidentales
En algunos pacientes, la alimentación IV se emplea para complementar la ingestión deficiente.
Los objetivos fundamentales son aportar calorías y nitrógeno suficientes para reparación de los tejidos y la conservación o el crecimiento de la masa de tejidos magros.
A continuación se enumeran situaciones en que se utiliza alimentación parenteral.
- Neonatos con anomalías gastrointestinales catastróficas, como fístula traqueoesofágica, gastrosquisis, onfalocele o atresia intestinal masiva.
- Lactantes con aumento insuficiente de peso de origen inespecífico o secundario a insuficiencia gastrointestinal por síndrome de intestino corto, malabsorción, déficit enzimáticos, ileo por meconio y diarrea idiopática.
- Adultos con síndrome de intestino corto por resección intestinal masiva o fístulas enteroentérica, enterocólica, enterovesical o enterocutánea.
- Pacientes con obstrucciones gastrointestinales sin afección vascular, por acalasia, estrecheces o neoplasias esofágicas, así como carcinoma gástrico u obstrucción pilórica.
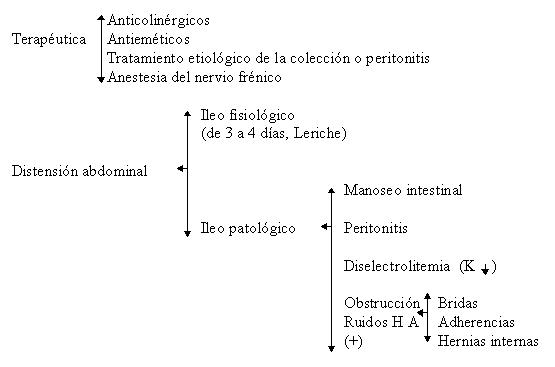
- Pacientes quirúrgicos con ileo paralítico prolongado después de cirugía mayor, lesiones múltiples o traumatismos abdominales penetrantes o no, además de pacientes con íleo reflejo o complicación de diversos trastornos médicos.
- Pacientes con longitud intestinal normal a la vez que malabsorción por Sprue, hipoproteinemia, insuficiencias enzimática o pancreática, enteritis regional o colitis ulcerativa.
- Adultos con trastomos gastrointestinales funcionales, como discinesia esofágica o accidentes cerebrovascular, diarrea idiopática, vómito psicógeno o anorexia nerviosa.
- Personas que no pueden ingerir alimentos o que los regurgitan o broncoaspiran después de ingerirlos o recibirlos por sonda a causa de la disminución total o parcial del nivel de conciencia por trastornos metabólicos graves, padecimientos neurológicos, cirugía intracraneal o traumatismos del sistema nervioso central.
- Sujetos con hipermetabolismos por traumatismos graves, como las quemaduras extensas de tercer grado, fracturas de importancia o lesiones de tejidos blandos.
- Individuos que padecen colitis granulomatosa o ulcerativa y enteritis tuberculosa, en que está enferma la porción principal de la mucosa de absorción.
- Parapléjicos, cuadripléjicos o debilitados con úlceras por decúbito indoloras en el area pélvica, en particular cuando hay contaminación fecal.
- Personas con cáncer, acompañado o no de caquexia, en quienes la desnutrición puede poner en riesgo el éxito de una modalidad terapéutica contra el tumor.
- Personas con insuficiencia renal aguda reversible, en quienes el hipercatabolismo origina la liberación de aniones y cationes intracelulares que inducen hipercaliemia, hipermagnesemia o hiperfosfatemia.
COLOCACION DEL CATETER VENOSO CENTRAL
El éxito de la hiperalimentación IV por lo general depende de la colocación y conservación correcta del catéter venoso central. Este, radiopaco, de calibre 16 fr y 20-30 cm de longitud, se introduce de manera percutánea hasta las venas subclavia o yugular interna, por las que se llega hasta la cava superior.
La introducción del cateter en la subclavia empieza con la colocación del paciente sobre su espalda, con la cabeza en un ángulo de 15º debajo de la horizontal y una pequeña almohadilla entre los omóplatos, que permite el descenso de los hombros en sentido posterior y con esto, la dilatación de la subclavia. La piel se limpia con éter y después con un yodoforo. Luego se colocan lienzos quirúrgicos adecuados y se acatan las medidas de asepsia. Se infiltra un anestésico local en la piel, tejido subcutáneo y periostio a la altura del borde inferior del punto medio de la clavícula. Se introduce una aguja del 14 Fr. de 5 cm de longitud, acoplada a una jeringa en el sitio de punción, con el bisel hacia abajo, y se adelanta hacia la punta del dedo del operador. La aguja ha de pasar junto a la superficie clavicular inferior, arriba de la primera costilla hacia la subclavia. Su entrada en la vena se advierte por la presencia de sangre cuando se aspira con la jeringa. La aguja se adelanta unos cuantos milímetros más para cerciorarse de que esté por completo en el interior de la vena.
Después, se pide al paciente que realice la maniobra de Valsalva o se presiona con el pulgar sobre el sitio de punción mientras se extrae la jeringa, para prevenir la embolia gaseosa. A continuación, se introduce un catéter radiopaco 16 fr de 20-30 cm por la aguja y se lleva hasta la vena cava superior.
El paso siguiente es extraer la aguja y acoplar una pequeña férula de plástico en la unión del catéter con la aguja, para evitar que ésta corte al catéter. En siguiente término, se conecta el catéter con un tubo esterilizado para venoclisis y se comienza la administración lenta mientras se sutura el catéter a la piel y se cubre éste con un apósito oclusivo.
Se toma una radiografía torácica para confirmar la posición del cateter radiopaco en la vena cava y la ausencia del posible neumotórax.
Cada dos o tres días en el sitio de punción se cambia el tubo de venoclisis, se procede a la asepsia quirúrgica y se aplica ungüento antibiótico y un nuevo apósito oclusivo.
El uso de la yugular interna ha sido muy satisfactorio especialmente en niños. No es prudente a menos que resulte del todo necesario, llevar catéteres hasta la vena cava inferior desde las extremidades inferiores, en virtud de las mayores probabilidades de sepsis y tromboembolia.
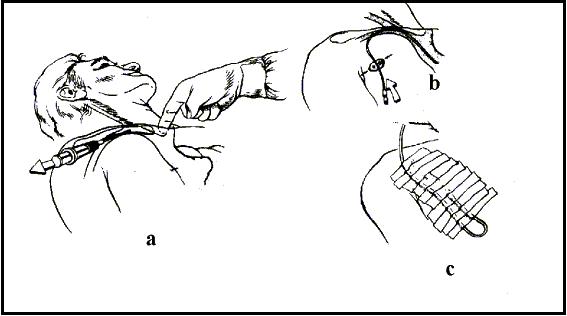
PUNCION SUBCLAVIA
a. Introducción del trocar de punción subclavia, previa antisépsia y anestesia local.
b. Colocación del catéter a través del trocar
c. Apósito oclusivo.
PREPARACION Y ADMINISTRACION DE LAS SOLUCIONES
La solucion básica tiene una concentración final de 20-25% de dextrosa y 3-5% de aminoácidos cristalinos.
Los preparados vitamínicos IV se deben agregar, además hay que agregar 10mg de fitomenadiona, (vitamina k) y 5 mg de ácido fólico por vía IM una vez por semana, dado que son inestables en la solucion de hiperalimentación. También se prescribe una inyeccion IM mensual de cianocobalamina (vitamina B12)
La deficiencia de ácidos grasos esenciales se torna evidente con dermatitis, sequedad de piel, descamación, caida del cabello. Este síndrome se previene con la administración de una emulsión de grasas equivalente al 4-5 % del total de calorías aportadas.
Las emulsiones de grasa que aportan 9kcal/g, dos veces más que las calorías suministradas por lg de glucosa, son isotónicas y pueden administrarse a través de una vena periférica, estas emulsiones contienen aceite de soja o de semillas de algodón y están constituidas principalmente por los ácidos oleico y linoleico.
Se suelen requerir oligoelementos minerales esenciales y es factible suministrarlos por la adicion directa de sus preparados comerciales a las soluciones de aminoácidos y dextrosa.
Se adiciona además cloruro de zinc (su deficit produce exantema eczematoide) y sulfato de cobre (su deficit produce anemia microcítica). el deficit de cromo produce intolerancia a la glucosa.
La insulina se administra para garantizar la tolerancia a la glucosa, es fundamental agitar el frasco en donde se la diluye, pues su depósito por la gravedad puede producir hipoglucemias severas.
Es imperativa la vigilancia minuciosa en busca de complicaciones electrolíticas, volumétricas, acidobásicas y sépticas. Los signos vitales y diuresis se miden con regularidad, además se pesa diariamente al enfermo.
Los ajustes frecuentes del volumen y composición de las soluciones son necesarias durante el tratamiento. Los electrólitos se miden cada día hasta que se recupere la estabilidad y cada dos o tres días en lo sucesivo, ademas de medir al menos en forma semanal el hemograma, BUN, funciones hepáticas, fosfato y magnesio.
La glucosuria se mide cada 6h y la glucemia por lo menos una vez diaria durante los primeros días del régimen.
La insulina se administra en la medida necesaria para mejorar la tolerancia a los cabohidratos. La respuesta de la glucemia a la insulina exógena se evalúa por medición frecuente en sangre capilar. Si persisten la hiperglucemia o glucosuria, es usual que se disminuya la concentración de dextrosa en la solución, se desacelere la velocidad de administración de esta o se agregue insulina como respuesta a la administración continua de carbohidratos.
La administración de concentraciones adecuadas de potasio es indispensable para lograr el balance nitrogenado positivo y reponer las reservas intracelulares disminuidas de este ion. Además el desplazamiento significativo del potasio, del medio extracelular a intracelular, suele ocurrir a causa de la administración considerable de glucosa, lo que da lugar a hipocaliemia, alcalosis metabólica y aprovechamiento deficiente de la glucosa.
La hipocaliemia puede causar glucosuria, que se trata con potasio, no con insulina.
EMULSIONES DE LIPIDOS
Las emulsiones de lípidos derivados de los aceites de soja y girasol se emplean como nutriente coadyuvante para prevenir el déficit de ácidos grasos esenciales.
Por otra parte, son eficaces los lípidos como fuente de calorías en personas con traumatismos e hipermetabolismo. Se aconseja limitar las emulsiones referidas a 2,0-2,5 g/kg/día.
En caso de carecer de estas emulsiones para administración EV, por su costo, se puede intentar suplementar el aporte calórico y de ácidos grasos esenciales mediante la aplicación de aceites vegetales sobre la superficie cutánea, siendo de este modo difícil cuantificar la real absorción.
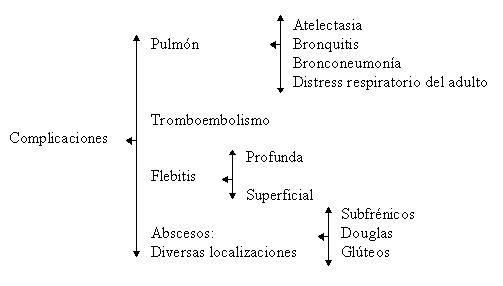
COMPLICACIONES
Una de las complicaciones más graves es la sepsis bacteriana o micótica por contaminación del catéter venoso central.
Uno de los primeros signos de la sepsis generalizada suele ser la aparición súbita de intolerancia a la glucosa (con o sin hipertermia), estando indicada la búsqueda minuciosa de un foco séptico.
Si persiste la fiebre hay que extraer el catéter venoso y realizar cultivos del mismo, actualmente en algunos centros clínicos se reemplazan los catéteres de pacientes con bajo riesgo de infección mediante un alambre guía en J. En caso de persistir infección 24-48 hs sin causa definida, reemplácese el catéter en la subclavia opuesta o en yugular interna.
Otras complicaciones relacionadas con la introducción del catéter son el neumotórax, hemotórax e hidrotórax, lesiones de la arteria subclavia; arritmias cardíacas si el catéter se lleva hasta la aurícula o el ventrículo, embolia gaseosa por catéter y en unos casos perforación cardíaca y taponamiento.
La tomboflebitis o trombosis clínicamente evidentes de la vena cava superior han sido raras.
Hay una tendencia al uso cada vez más frecuente de catéteres de luz múltiple para la alimentación parenteral y la vigilancia de pacientes gravemente enfermos. El uso de catéteres implantados en forma permanente se reserva para pacientes sin sepsis o de alto riesgo que requieran nutrición o fluidoterapia durante largos periodos, así como otros enfermos seleccionados en quienes se precisen valoraciones sanguíneas frecuentes.